Nacional
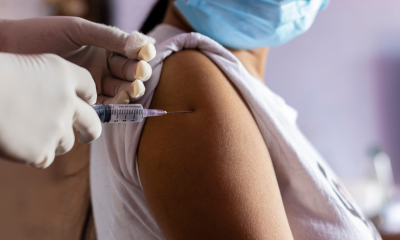
Entenda a MP editada por Bolsonaro que facilita regras de aquisição de vacinas

![]()

O presidente Jair Bolsonaro editou nesta quarta-feira (6) a Medida Provisória (MP) 1026/21, que flexibiliza regras para facilitar a aquisição de vacinas e insumos. O texto possibilitará a aquisição de insumos e vacinas em fase de desenvolvimento e antes do registro sanitário ou de autorização de uso emergencial pela Agência Nacional de Vigilância Sanitária (Anvisa). A ideia do governo é dinamizar o processo de aquisição de vacinas.
Além disso, a MP flexibiliza normas de licitação, possibilitando que as partes estabeleçam termos contratuais sobre eventual pagamento antecipado, inclusive com a possibilidade de perda do valor antecipado, hipóteses de não penalização da contratada, bem como outras condições indispensáveis para obter o bem ou assegurar a prestação do serviço.
O texto também firma o Plano Nacional de Operacionalização da Vacinação contra a Covid-19 como “instrumento estratégico” de vacinação de toda a população. A MP também determina que o profissional de saúde esclareça ao paciente ou seu representante legal que o produto não tem registro definitivo na Anvisa, assim como seus riscos e benefícios.
Os estabelecimentos de saúde, públicos e privados, deverão registrar, diariamente e de forma individualizada, os dados referentes à aplicação de vacinas contra a covid-19 , assim como de eventuais efeitos colaterais, em um sistema de informação que será disponibilizado pelo Ministério da Saúde.
Pelo texto, a Anvisa poderá conceder autorização excepcional e temporária para a importação e distribuição de quaisquer vacinas contra a covid-19 , além de materiais, medicamentos, equipamentos e insumos da área de saúde sujeitos à vigilância sanitária, que não tenham registro na agência desde que esses produtos sejam registrados por, no mínimo, uma autoridade sanitária estrangeira e autorizados à distribuição em seus respectivos países.
As agências estrangeiras selecionadas pela Anvisa são: Food and Drug Administration – FDA (EUA); European Medicines Agency – EMA (União Europeia); Pharmaceuticals and Medical Devices Agency – PMDA (Japão); National Medical Products Administration – NMPA (China) e Medicines and Healthcare Products Regulatory Agency – MHRA (Reino Unido).
Ainda não existem vacinas registradas pela Anvisa . Laboratórios produtores de vacina e seus parceiros no Brasil têm se reunido com a agência reguladora e tratado da documentação necessária para fazer o pedido de uso emergencial da vacina.
A MP foi publica em edição extra do Diário Oficial da União nesta sexta-feira. A edição extra também traz o despacho do presidente da República que envia o texto para o Congresso Nacional.
-

 Meio Ambiente28/06/2024
Meio Ambiente28/06/2024Pantanal: 85% dos incêndios ocorrem em terras privadas, diz Marina
-

 Ministério Público28/06/2024
Ministério Público28/06/2024Justiça determina repasse mensal de recursos para manutenção de maternidades da capital
-

 Economia28/06/2024
Economia28/06/2024Lula sanciona taxação de compras internacionais de até 50 dólares
-

 Saúde28/06/2024
Saúde28/06/2024Tocantins discute ações para evitar mortalidade materna e infantil no estado
-

 Direitos Humanos29/06/2024
Direitos Humanos29/06/2024Dia do Orgulho LGBTQIA+: país tem longa história de luta por direitos
-

 Oportunidade28/06/2024
Oportunidade28/06/2024Autorizado concurso para 1,6 mil vagas na Polícia Penal
-

 Cidades28/06/2024
Cidades28/06/2024PCGO e PCDF prendem no DF foragido por homicídio ocorrido em Caldas Novas
-

 Meio Ambiente29/06/2024
Meio Ambiente29/06/2024Quase 1/4 do território brasileiro pegou fogo nos últimos 40 anos